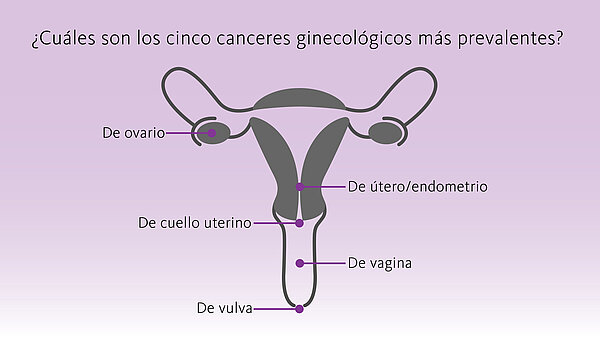
Soluções diagnósticas em cancros ginecológicos: trazer à luz com precisão o que precisa de ser visto
As doenças malignas que afetam os órgãos reprodutores femininos são conhecidas como “cancros ginecológicos”. Representam anualmente aproximadamente 1,4 milhões de novos casos e são responsáveis por 700.000 mortes anuais em todo o mundo, sendo os cancros do colo do útero, endométrio e ovário os mais frequentemente diagnosticados. [1]
A detecção precoce de cancros ginecológicos, o seu diagnóstico e estadiamento precisos, bem como o seu tratamento desempenham um papel fundamental no prognóstico/resultado e na qualidade de vida da doente.
Nos últimos anos, as abordagens diagnóstica e cirúrgica têm sido mais personalizadas, resultando em tratamentos menos invasivos. Isso também se deve ao estabelecimento do conceito de gânglio linfático sentinela e ao aumento da aplicação de testes de genética molecular para diagnóstico, permitindo melhor caracterização e compreensão do cancro, do seu comportamento e agressividade, bem como do risco e do prognóstico para cada doente. Todos estes fatores apoiam a seleção do tratamento mais adequado.
Oferecemos uma gama de soluções baseadas em tecnologias de ponta em biologia molecular que auxiliam os profissionais de saúde e os doentes durante todo o processo de recuperação.
Um padrão de estadiamento mais flexível
Durante o tratamento de muitos cancros ginecológicos, é importante avaliar se o mesmo se espalhou para os gânglios linfáticos. Os primeiros, para onde é mais provável que as células oncológicas se possam ter disseminem, são designados por gânglios sentinela, em inglês “sentinel lymph nodes” (SLN). Uma biópsia a estes gânglios sentinela ajudará a determinar o estadiamento oncológicos e, como tal, o plano de tratamento individual.
A utilização do sistema de localização magnética Sentimag® – Magtrace® ajuda a identificar eficazmente os gânglios sentinela, evitando os problemas associados aos materiais radioativos. [2-3]
Procedimento
Para poder identificar os gânglios sentinela durante a cirurgia, o cirurgião injeta uma pequena quantidade (até 2 ml) de Magtrace® perto do cancro. Após a injeção, o localizador Magtrace® fluirá através do sistema linfático até marcar os gânglios linfáticos sentinela.
A injeção pode ser administrada 30 dias antes da cirurgia ou no próprio bloco operatório logo após a administração da anestesia. Durante o procedimento cirúrgico, o cirurgião utilizará a sonda Sentimag® para identificar os gânglios sentinela marcados que serão retirados e encaminhados para o laboratório de patologia para análise.
Benefício
O localizador Magtrace® é uma técnica estabelecida, utilizada em mais de 65.000 procedimentos cirúrgicos em todo o mundo, que permite maior flexibilidade e conveniência para doentes e médicos, uma vez que pode ser injetado numa janela de 30 dias.
Endomag®, Sentimag® e Magseed® são marcas registadas da Endomagnetics Ltd na União Europeia
Magtrace® é uma marca registada da Endomagnetics Ltd no Reino Unido
Diagnóstico oncológico com OSNA
O estadiamento oncológico é um passo que ajuda a determinar o tipo e a extensão do tratamento adequado ao doente. Uma parte essencial do processo de estadiamento é a avaliação do estado ganglionar.
Revelar a imagem completa
O estado dos gânglios linfáticos é o parâmetro de estadiamento mais importante com valor prognóstico na gestão dos cancros ginecológicos. Quer os gânglios linfáticos estejam envolvidos ou não, o seu estado guia os médicos nas decisões sobre a abordagem cirúrgica mais adequada, sobre a extensão da intervenção cirúrgica e sobre que tipo de terapia adicional poderá ser necessária.
Os métodos histopatológicos atuais apresentam várias limitações, dado que não permitem facultar informação diagnóstica de confiança em cenários intraoperatórios e/ou apresentam falta de sensibilidade para obter um estadiamento preciso. Como resultado, há o risco de que metástases pequenas permaneçam indetetáveis, motivando resultados falsos negativos e tratamentos desadequados.
A técnica OSNA (amplificação de ácido nucleico num passo) permite uma avaliação molecular dos gânglios linfáticos mais rápida, sensível e padronizada, o que permite a determinação precisa do estado ganglionar. Ao analisar o gânglio linfático completo, o método OSNA proprociona um estadiamento preciso e uma base fiável para a tomada de decisões de tratamento adaptada ao doente, se necessário, durante a cirurgia, o que ajuda a prevenir o subtratamento ou sobretratamento e assegurar a qualidade de vida do doente.
O cancro do ovário é geralmente detetado em fases tardias sendo, de todos os cancros ginecológicos, o mais letal. O tratamento deste tipo de cancro melhorou ao longo dos últimos 30 anos, devido a um melhor foco cirúrgico e a uma melhor disponibilidade de tratamentos de quimioterapia. Tal acontece devido à introdução de fármacos baseados na platina e, recentemente, graças à adição dos taxanos. Apesar destas melhorias no tratamento, até 30% das doentes não apresentam remissão clínica. A maioria das mulheres acaba por apresentar recidivas, geralmente com doença incurável. [4] Apesar de a cirurgia e o tratamento da doença em fase precoce estarem associadas a uma melhoria da sobrevivência, é impossível prever que doentes irão recidivar ou apresentar progressão de doença durante ou após a quimioterapia. Esta previsão é essencial, já que as doentes com resistências podem beneficiar de uma combinação diferente de tratamentos [4], incluindo terapia dirigida moderna.
O desenvolvimento de testes genéticos permitiu uma melhor caracterização e compreensão do cancro do ovário, do seu comportamento e agressividade, bem como do risco e prognóstico da doente, o que apoia a seleção do tratamento adequado.
As mutações da linha germinal dos genes BRCA1 e BRCA2 conduzem a um maior risco de cancro do ovário. Representam os fatores de risco genético predominantes mais bem caracterizados e identificados para a doença até ao momento. As mutações BRCA1 e BRCA2 estão envolvidas em quase metade de todas as famílias com dois ou mais casos de cancro do ovário. Na medida que os genes BRCA1 e BRCA2 codificam as proteínas envolvidas na reparação do ADN, os tumores com alterações em qualquer dos genes são particularmente sensíveis aos agentes anticancerígenos específicos que atuam danificando o ADN. [5]
A avaliação do estado mutacional do tumor é decisiva na seleção de doentes para terapia dirigida. Para investigar essas alterações genéticas, os oncologistas podem fazer uso de uma ampla variedade de testes genéticos moleculares que os podem apoiar na tomada de decisões sobre o tratamento personalizado. A precisão aquando do diagnóstico é fundamental para selecionar a terapia certa no momento certo para a doente.
Testes moleculares para seleção de terapia
As sondas CytoCell FISH (hibridação in situ fluorescente) têm como alvo os genes MET, ROS1, CHD5, TOP2A e ZNF217. Estes são usados para ajudar patologistas e médicos a entender o comportamento/agressividade do tumor e, portanto, o prognóstico da doente.
BRCA1, BRCA2, TP53, PTEN, ATM, ATR e NF1 estão entre os genes germinais mais comuns e entre os genes somáticos mutados subjacentes à patogénese do cancro do ovário que podem ser investigados com testes de sequenciação de próxima geração (NGS). A solução da Sysmex que ajuda a caracterizar o contexto genómico geral do cancro do ovário é o painel de cancro do ovário SuresqTM.
Leia duas histórias inspiradoras de sobreviventes
Partilham palavras de inspiração, esperança e a forma como as suas vidas foram transformadas pela doença.
Saiba mais sobre como a Sysmex faz a diferença na luta contra os cancros ginecológicos
Descubre más

Referencias
- Sung H, et al. (2021) Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. PMID: 33538338
- Rzepka et al. (2014): Sentinel lymph node identification using a magnetic tracer for endometrial cancer: A pilot study. J Clin Oncol 32, 2014 (suppl; abstr e16550)
- Jedryka MA, Klimczak P, Kryszpin M, et al. (2020): Superparamagnetic iron oxide: a novel tracer for sentinel lymph node detection in vulvar cancer. Int J Gynecol Cancer, doi:10.1136/ ijgc-2020-001458
- Helleman J. et al., (2006) Molecular profiling of platinum resistant ovarian cancer. Int J Cancer 118(8):1963-71.
- Radu MR et al. (2021) Ovarian Cancer: Biomarkers and Targeted Therapy. Biomedicines. Jun 18;9(6):693. doi: 10.3390/biomedicines9060693.