Calendário científico setembro 2024
Uma abordagem integrada desde o rastreio até à monitorização de uma doença hemato-oncológica
Por que um diagnóstico rápido de LPA é crucial para o doente?
Para reduzir o custo do tratamento
Para prevenir o desenvolvimento de leucemia crónica
Para gerir e mitigar o alto risco de hemorragia grave
Para minimizar a duração do internamento hospitalar
Para melhorar a eficácia da quimioterapia
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Informação de contexto
A leucemia promielocítica aguda (LPA), um subtipo de leucemia mieloide aguda (LMA), é afetada pela presença do transcrito do gene de fusão PML-RARA [1,3]. A deteção precoce e o tratamento imediato são cruciais para os doentes com LPA devido ao risco de distúrbios fatais da coagulação e hemorragias potencialmente letais no momento do diagnóstico.
Antes da introdução do ácido totalmente trans-retinóico (ATRA) e do trióxido de arsénico (ATO) nos protocolos de tratamento, a LPA apresentava um mau prognóstico. No entanto, essas terapias melhoraram consideravelmente a taxa de sobrevivência geral e curaram quase 90% dos doentes [4]. Doentes com translocações de variante RARA apresentam sensibilidade variável ao tratamento, com alguns a mostrar resistência [2]. Portanto, é essencial distinguir entre doentes com LPA com fusão PML-RARA e aqueles com translocações de variante RARA.
No início do processo de diagnóstico, a amostra de sangue de um doente geralmente é verificada em busca de anormalidades, como contagens anormais de glóbulos brancos e/ou diferenciais anormais de glóbulos brancos. No caso de uma anormalidade, o exame morfológico dos glóbulos brancos no sangue periférico revela um grande promielócito atípico com núcleo localizado excentricamente, geralmente bilobado, com um contorno dobrado e nucléolo proeminente. Os promielócitos circulantes, assim como outros precursores mieloides em vários estágios, apresentariam grânulos azurófilos irregulares ou bastonetes de Auer [5].
Aproximadamente três quartos dos doentes apresentam, no momento do diagnóstico, coagulação consumptiva, que consiste em tempo de tromboplastina parcial (TTP), tempo de protrombina (TP) e dímeros D elevados, juntamente com hipofibrinogenemia e trombocitopenia [5]. O diagnóstico deve ser confirmado por citometria de fluxo e análise molecular.
A análise citométrica de fluxo de LPA mostra uma fenotipagem imunológica que inclui uma baixa expressão ou ausência de HLA-DR, CD34, CD11a, CD11b e CD18. Além disso, a expressão clara de CD33 é frequentemente observada com uma expressão mista de CD13. Muitos casos mostram expressão de CD117, embora tenda a ser fraca. 20% dos casos expressam CD56, que tem sido associado a um mau prognóstico.
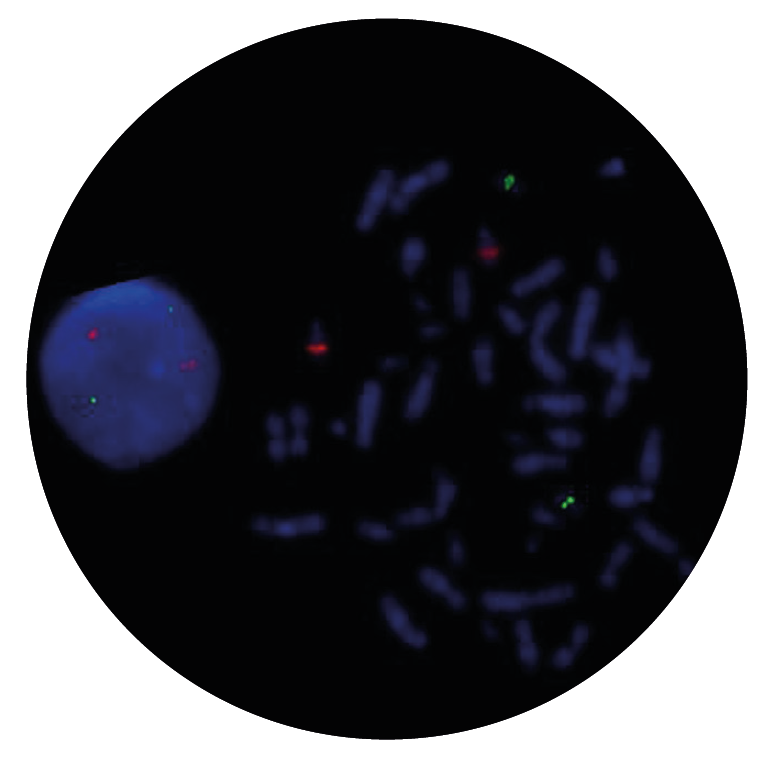
A hibridização in situ por fluorescência (FISH) é altamente sensível, tornando-se uma ferramenta importante para o diagnóstico de LPA através da identificação de translocações. A capacidade do FISH de proporcionar resultados rápidos e precisos é particularmente importante no contexto da LPA, onde o início oportuno do tratamento apropriado pode salvar vidas.
Referências
[1] Bruneau J (2019): WHO classification of tumors of hematopoietic and lymphoid tissues. Hematopathology: 501-505.
[2] Creutzig U et al. (2012): Diagnosis and management of acute myeloid leukemia in children and adolescents: recommendations from an international expert panel. Blood. The Journal of the American Society of Hematology 120.16: 3187-3205.
[3] Jimenez JJ et al. (2020): Acute promyelocytic leukemia (APL): a review of the literature. Oncotarget 11.11: 992.
[4] Tomita, Akihiro, Hitoshi Kiyoi, and Tomoki Naoe. (2013): Mechanisms of action and resistance to all-trans retinoic acid (ATRA) and arsenic trioxide (As 2 O 3) in acute promyelocytic leukemia. International journal of hematology 97: 717-725.
[5] Yilmaz M et al. (2021): Acute promyelocytic leukemia current treatment algorithms. Blood Cancer Journal. 11:123.